 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站! 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站!
Ø 研究背景
肝细胞癌(HCC)是全球重大健康负担,预后极差,亟需阐明驱动其进展的新机制。HCC细胞呈现有氧糖酵解(Warburg效应)特征,产生大量乳酸。近年发现的组蛋白乳酸化修饰(特别是H3K18la)可连接糖酵解与基因转录,但其特异性"阅读器"蛋白长期未知。BRD9是ncBAF染色质重塑复合物的核心亚基,通过溴结构域识别酰化修饰促进染色质开放。鉴于HCC对ncBAF的依赖性及BRD9的修饰识别特性,本研究旨在探究BRD9是否作为H3K18la的阅读器,将代谢信号转化为染色质重塑事件,为HCC治疗提供新靶点。
Ø 研究结果
通过对HCC患者配对的肿瘤与癌旁组织进行Western blot和免疫组化分析,发现肿瘤组织中pan-Kla和H3K18la水平显著高于癌旁组织,且与肿瘤分期进展和患者总生存期缩短强相关。在HCC细胞系中,H3K18la水平与糖酵解关键酶HK-2表达及细胞内乳酸含量正相关。通过糖酵解抑制剂(2-DG)和LDHA/LDHB敲低实验证实,糖酵解活性直接调控H3K18la水平,且糖酵解抑制可显著抑制HCC细胞增殖、克隆形成和迁移能力,外源性乳酸补充可部分逆转这些效应,确立了糖酵解-H3K18la-恶性表型的因果联系。

利用生物素标记H3K18la肽段的亲和纯化-质谱技术筛选相互作用蛋白,BRD9被鉴定为顶级候选蛋白。通过生物素pull-down、免疫共沉淀和体外重组蛋白结合实验,证实BRD9特异性识别H3K18la而非其同源蛋白BRD7,且该识别依赖于其溴结构域。进一步通过代谢干预实验(乳酸处理增强、糖酵解抑制减弱)和BRD9溴结构域抑制剂(BI-9564)阻断实验,证实BRD9作为代谢敏感型表观遗传阅读器,其染色质募集受糖酵解状态动态调控。

运用NMR波谱、表面等离子体共振(SPR)和等温滴定量热法(ITC)等技术,定量解析BRD9溴结构域与H3K18la的相互作用特征。结果显示BRD9对H3K18la的亲和力(KD≈363μM)约为H3K18ac(KD≈78μM)的5倍,提示其为弱而短暂的结合模式。NMR结构解析揭示,H3K18la通过保守的乙酰赖氨酸口袋与BRD9结合,乳酸基团的羰基氧与Asn216形成氢键,但较大的乳酸基团导致结合浅于乙酰基团,这解释了亲和力差异的结构基础。H3K18la结合诱导BRD9的BC环发生特异性构象变化,阐明BRD9作为动态代谢传感器的分子机制。

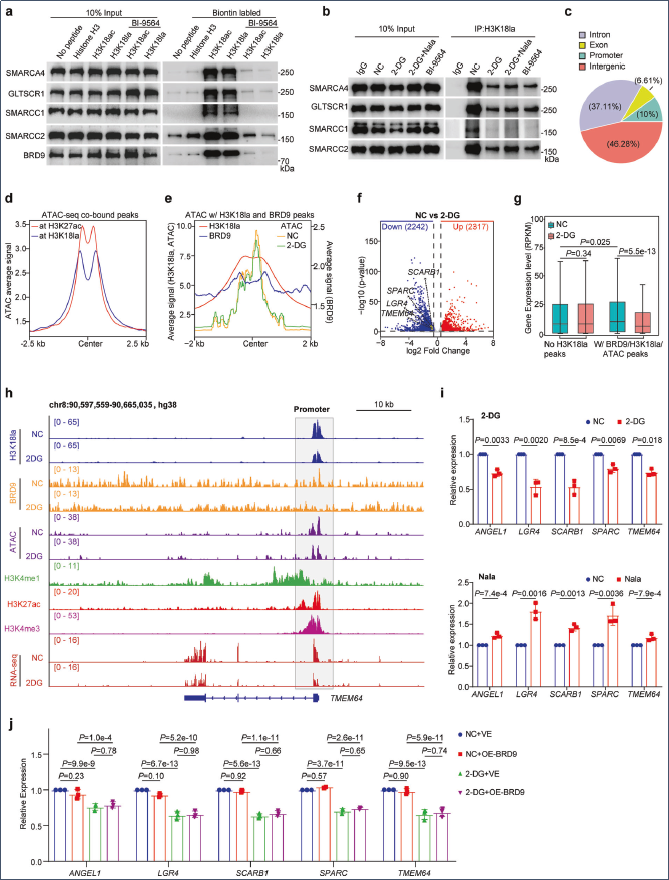
通过ChIP-seq全基因组定位分析,发现H3K18la主要分布于基因间区和内含子区域,与H3K27ac/H3K4me1标记的活性增强子及H3K27ac/H3K4me3标记的活性启动子显著重叠。BRD9 ChIP-seq显示23%的结合位点与H3K18la共定位,这些位点富集于Wnt、Hippo等肿瘤进展相关通路。糖酵解抑制导致H3K18la和BRD9在代表性位点(CT70、SPARC增强子,TMEM64启动子)的占据显著降低,且BRD9过表达无法挽救此效应,证实H3K18la对BRD9染色质募集的必要性,而非充分性。

H3K18la肽段pull-down实验可捕获ncBAF复合物核心亚基(GLTSCR1、SMARCA4、SMARCC1、SMARCC2),该相互作用受糖酵解状态和BRD9溴结构域活性调控。ATAC-seq分析显示78%的BRD9/H3K18la共结合峰与开放染色质区域重叠,糖酵解抑制优先降低这些位点的染色质可及性。RNA-seq鉴定出2242个糖酵解抑制下调基因,其中46.1%的BRD9/H3K18la/ATAC共靶向基因(ANGEL1、LGR4、SCARB1、SPARC、TMEM64)表达受抑,且BRD9过表达无法挽救其表达,确立H3K18la-BRD9-ncBAF轴在维持致癌转录中的核心作用,且该作用位于BRD9上游。
通过p300敲低/抑制(C646)和HDAC抑制(SAHA、LMK235)实验,证实p300是H3K18la主要转移酶,HDAC介导其去除,形成动态平衡。靶向该平衡(p300抑制或HDAC抑制)均可抑制HCC细胞活力和克隆形成。BRD9溴结构域抑制剂BI-9564或siBRD9敲低可阻断BRD9染色质占据,抑制靶基因表达和细胞存活。体内HepG2异种移植瘤实验中,糖酵解抑制剂2-DG(500 mg/kg)治疗使肿瘤体积减少46%、重量减少30%,伴随H3K18la水平和靶基因表达降低,且无显著系统毒性,证实靶向该代谢-表观遗传轴具有治疗HCC的潜力。

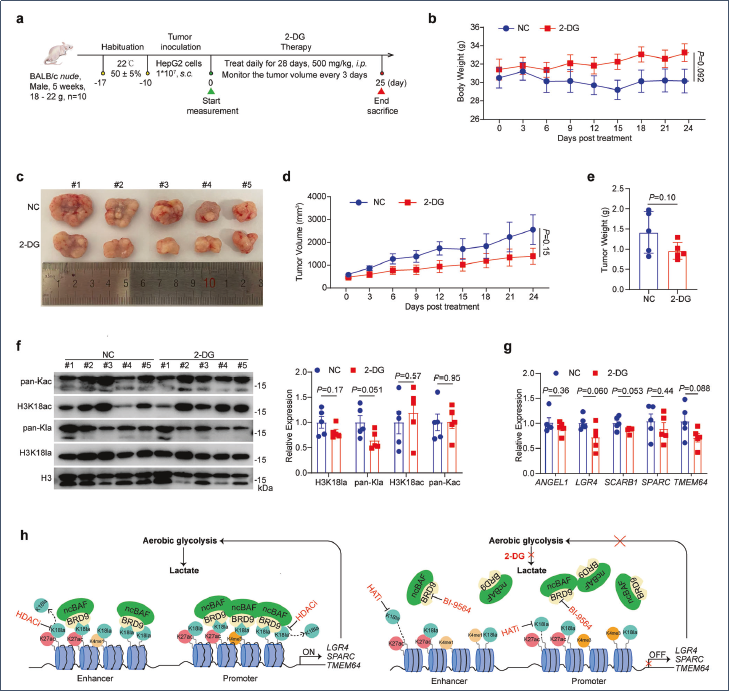
Ø 研究结论
本研究首次鉴定BRD9为组蛋白H3K18乳酸化的阅读器蛋白,阐明其通过溴结构域以弱亲和力动态识别H3K18la,将糖酵解代谢信号转化为ncBAF染色质重塑复合物的染色质募集,促进增强子/启动子开放并驱动致癌基因(ANGEL1、SPARC、TMEM64等)转录,形成"糖酵解-H3K18la-BRD9-ncBAF-致癌转录"的正反馈环路;靶向该轴(糖酵解抑制2-DG或BRD9抑制BI-9564)可有效抑制HCC细胞存活和体内肿瘤生长,为HCC的代谢-表观遗传联合治疗提供了新策略和理论框架。