 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站! 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站!《LRRK2 G2019S突变通过Drp1-STX17依赖的方式导致线粒体转移功能障碍》LRRK2 G2019S突变通过增强Drp1 Ser616磷酸化,导致STX17从线粒体脱落,从而损害星形胶质细胞向多巴胺能神经元的线粒体转移功能,而抑制Drp1磷酸化的DUSP6可恢复这一过程并发挥神经保护作用。成果发表在Translational Neurodegeneration杂志(IF:15.2);
原文链接:https://link.springer.com/article/10.1186/s40035-025-00525-1
《Translational Neurodegeneration》是一本专注于神经退行性疾病领域的开放获取、同行评议的英文学术期刊。期刊创刊于2012年1月,由上海交通大学医学院附属瑞金医院神经科、神经病学研究所与施普林格·自然集团合作创办。涵盖所有神经退行性疾病的相关研究,包括但不限于帕金森病及运动障碍、阿尔茨海默病及其他痴呆、运动神经元病等。感兴趣的主题包括流行病学、病原学、诊断标志物、新药开发、治疗及预防等。影响因子为15.2,5年影响因子为15.0;由BioMed Central出版,电子标准连续出版物号为 2047-9158;
帕金森病是仅次于阿尔茨海默病的第二大神经退行性疾病,其主要病理特征是中脑黑质区多巴胺能神经元的进行性丧失。尽管目前以多巴胺替代疗法为主的对症治疗能够改善症状,但无法阻止或延缓疾病的进展,因此探索能够抑制神经元凋亡的内源性神经保护机制具有重要意义。遗传因素和环境因素共同参与了帕金森病的发生。其中,LRRK2 G2019S突变是常见的帕金森病致病基因变异,可显著增强LRRK2激酶活性,导致线粒体自噬障碍、线粒体DNA损伤和线粒体分裂异常等病理改变。同时,前期研究已证实,星形胶质细胞可以将健康的线粒体转移给受损的多巴胺能神经元,这可能是脑内一种内源性的神经修复机制。然而,在LRRK2 G2019S突变背景下,这种线粒体转移功能是否受损,以及其具体分子机制尚不清楚。
研究方法:
研究采用诱导多能干细胞技术,从健康个体和携带LRRK2 G2019S突变的帕金森病患者外周血中成功诱导分化获得多巴胺能神经元和星形胶质细胞,建立了模拟脑内微环境的“星形胶质细胞-神经元”共培养体系。通过鱼藤酮处理模拟环境毒素暴露,实验首先观察了不同基因背景下线粒体转移效率的变化;进而利用MitoTracker标记星形胶质细胞线粒体,结合激光共聚焦显微镜和流式细胞术,定量检测共培养体系中神经元内星形胶质细胞来源的线粒体数量,并测定神经元ATP水平以评估其功能状态。在分子机制探讨层面,通过siRNA技术分别敲低SNARE家族蛋白STX17、VAMP3和SNAP23,筛选影响线粒体释放的关键蛋白;运用免疫荧光共定位分析STX17与线粒体外膜蛋白TOM20的共定位关系;采用免疫共沉淀技术验证Drp1与STX17的相互作用;并通过Western blot检测不同处理下Drp1总蛋白及其Ser616位点磷酸化水平的变化。,使用Drp1磷酸化抑制剂DUSP6进行功能挽救实验,观察其对STX17线粒体定位、线粒体转移效率及神经元树突损伤的改善作用。
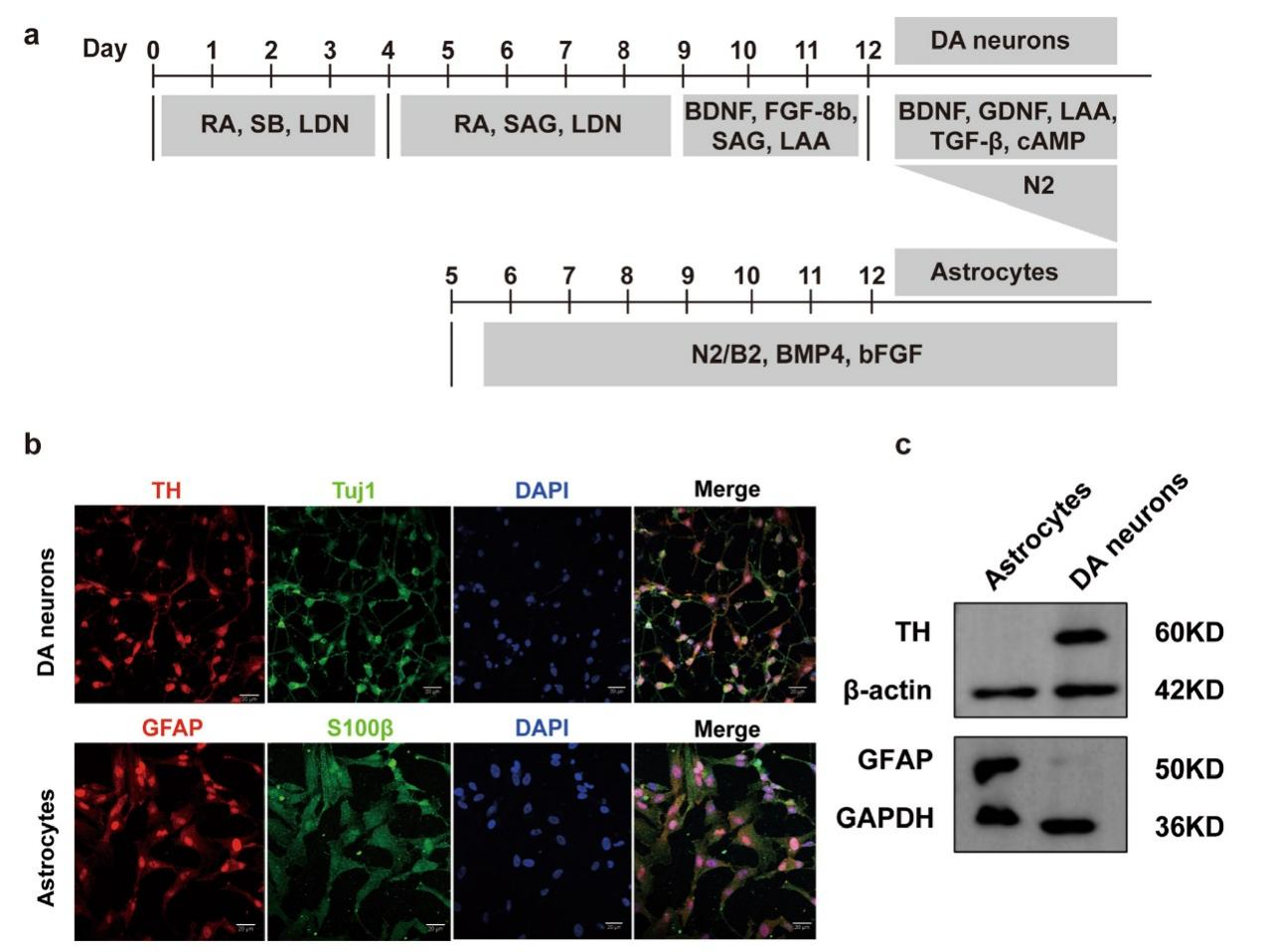
iPSCs来源于健康供体和携带LRRK2 G2019S杂合突变帕金森病患者的PBMCs,该患者是我团队报道的中国首例携带LRRK2 G2019S突变的帕金森病病例[31]。iPSCs的核型分析显示正常的46XY核型,无染色体异常。初,使用双重抑制剂SB431542和Noggin抑制SMAD信号通路,诱导iPSCs神经化为NSCs。通过向培养体系中添加各种小分子,成功实现了向星形胶质细胞和多巴胺能神经元的分化。并通过Western blot和免疫荧光对两种细胞的标志物进行验证。
2. LRRK2 G2019S突变减少线粒体从星形胶质细胞向多巴胺能神经元的转移
在突变型共培养体系(突变星形胶质细胞+突变神经元)中,200 nM鱼藤酮处理后神经元树突长度减少约60%,损伤程度显著重于野生型共培养体系(减少44%),表明突变神经元对环境毒素的抵抗力降低。当野生型星形胶质细胞与突变神经元共培养时,树突长度减少约50%,损伤轻于突变共培养体系,提示健康星形胶质细胞能部分缓解突变神经元的损伤。MitoTracker线粒体示踪显示,鱼藤酮呈剂量依赖性地减少神经元内星形胶质细胞来源的线粒体数量,突变体系中线粒体数量减少70%,野生型减少60%,说明突变导致线粒体转移功能受损更严重。流式细胞术检测星形胶质细胞条件培养基证实,突变星形胶质细胞释放线粒体的能力下降更明显。此外,将鱼藤酮处理后的条件培养基与神经元共培养发现,突变神经元ATP水平下降更显著,表明线粒体转移功能受损导致神经元能量供应不足。这些结果共同揭示了LRRK2 G2019S突变通过损害线粒体转移增强神经元对环境毒素的敏感性。
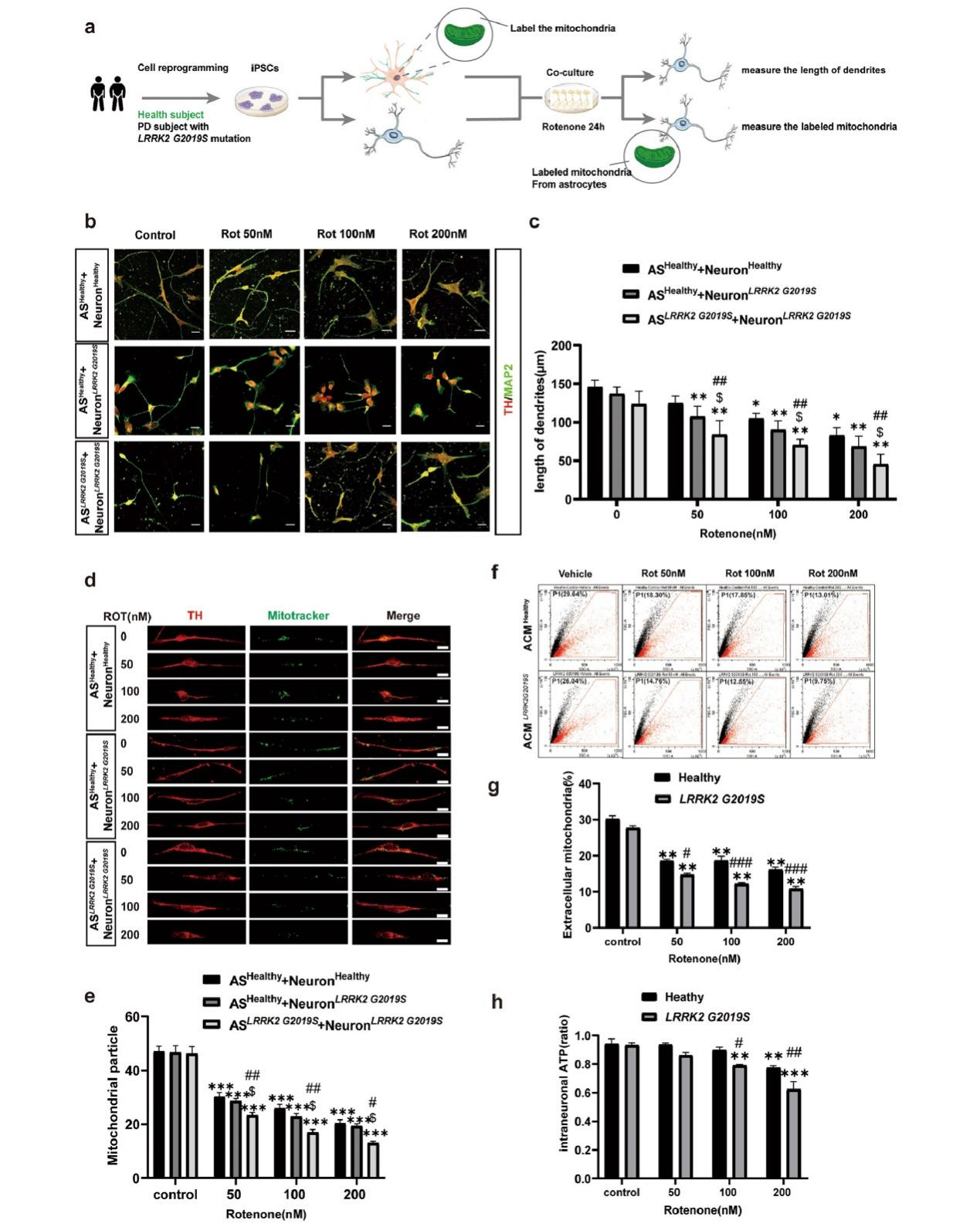
图2,LRRK2 G2019S突变与鱼藤酮联合作用导致多巴胺能神经元变性,并损害线粒体从星形胶质细胞向多巴胺能神经元的转移
3. 膜融合相关蛋白STX17通过不依赖SNARE的机制参与线粒体输出
通过siRNA分别敲低STX17、VAMP3和SNAP23后发现,STX17敲低使星形胶质细胞条件培养基中线粒体数量减少70.70%,而VAMP3和SNAP23敲低仅减少约27%,表明STX17是线粒体释放的关键调控蛋白。免疫共沉淀显示VAMP3与STX17、SNAP23均无结合,免疫荧光进一步证实STX17与线粒体外膜蛋白TOM20共定位,而VAMP3和SNAP23不与TOM20共定位,证明STX17的作用不依赖经典SNARE复合物形成。在鱼藤酮处理的星形胶质细胞中,STX17与TOM20的共定位程度随鱼藤酮浓度升高而降低,且突变型星形胶质细胞中这种下降更为显著。值得注意的是,线粒体标志物TOM20和VDAC1的蛋白水平在不同基因型和不同浓度鱼藤酮处理下均无显著变化,表明线粒体数量保持稳定,排除了线粒体自噬或降解对共定位结果的影响。然而,200 nM鱼藤酮使野生型星形胶质细胞STX17荧光强度降低27%,突变型降低41%,Western blot验证了这一结果。进一步的共定位分析证实,STX17定位于线粒体外膜的能力下降是导致线粒体转移功能受损的直接原因。这些结果揭示了STX17在线粒体释放中的关键作用及其受突变和环境毒素协同调控的机制。
图3的核心研究发现是STX17通过不依赖经典SNARE复合物的机制参与星形胶质细胞线粒体释放,且LRRK2 G2019S突变与鱼藤酮协同损害STX17的线粒体定位。
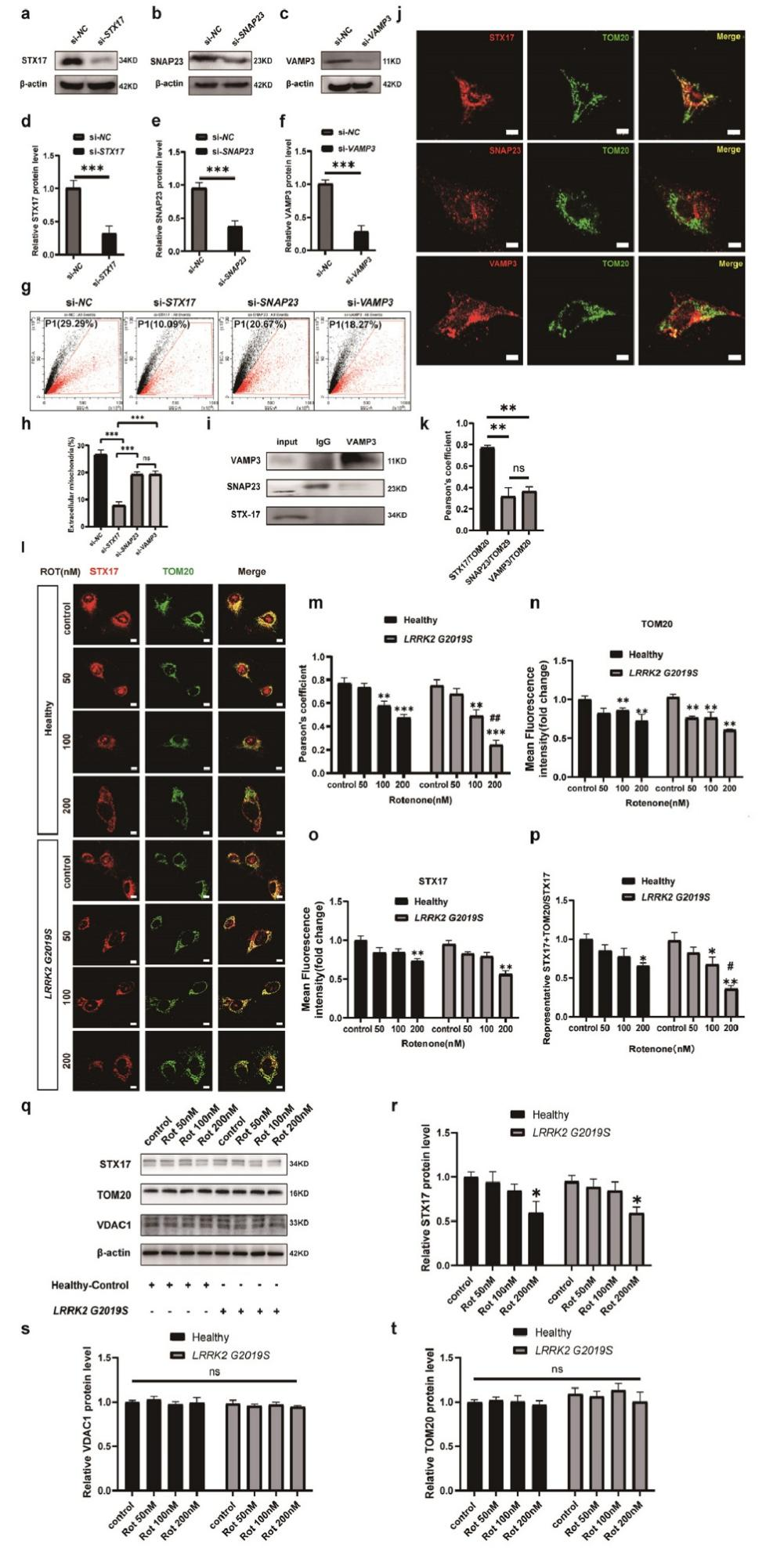
图3,STX17通过不依赖SNARE的机制参与星形胶质细胞的线粒体输出
通过siRNA敲低Drp1后,星形胶质细胞条件培养基中线粒体数量显著减少,共培养体系中神经元内星形胶质细胞来源的线粒体也明显减少,证实Drp1是线粒体释放的关键调控蛋白。免疫共沉淀结果显示,Drp1与STX17存在直接相互作用,为Drp1调控STX17功能提供了分子基础。进一步检测发现,随着鱼藤酮浓度升高,Drp1 Ser616位点磷酸化水平呈剂量依赖性增加,且突变型星形胶质细胞中这一磷酸化水平在各浓度下均显著高于野生型,尤其在200 nM鱼藤酮处理下差异为明显。值得注意的是,总Drp1蛋白水平在两种基因型和不同鱼藤酮浓度下均无显著变化,表明突变和毒素主要影响Drp1的磷酸化状态而非表达量。这些结果共同揭示:LRRK2 G2019S突变增强Drp1 Ser616磷酸化,这种过度磷酸化可能干扰Drp1与STX17的正常相互作用,进而导致STX17从线粒体脱落,终损害线粒体转移功能。该发现阐明了从遗传突变到分子事件再到功能损伤的关键通路,为后续药物干预提供了明确靶点。
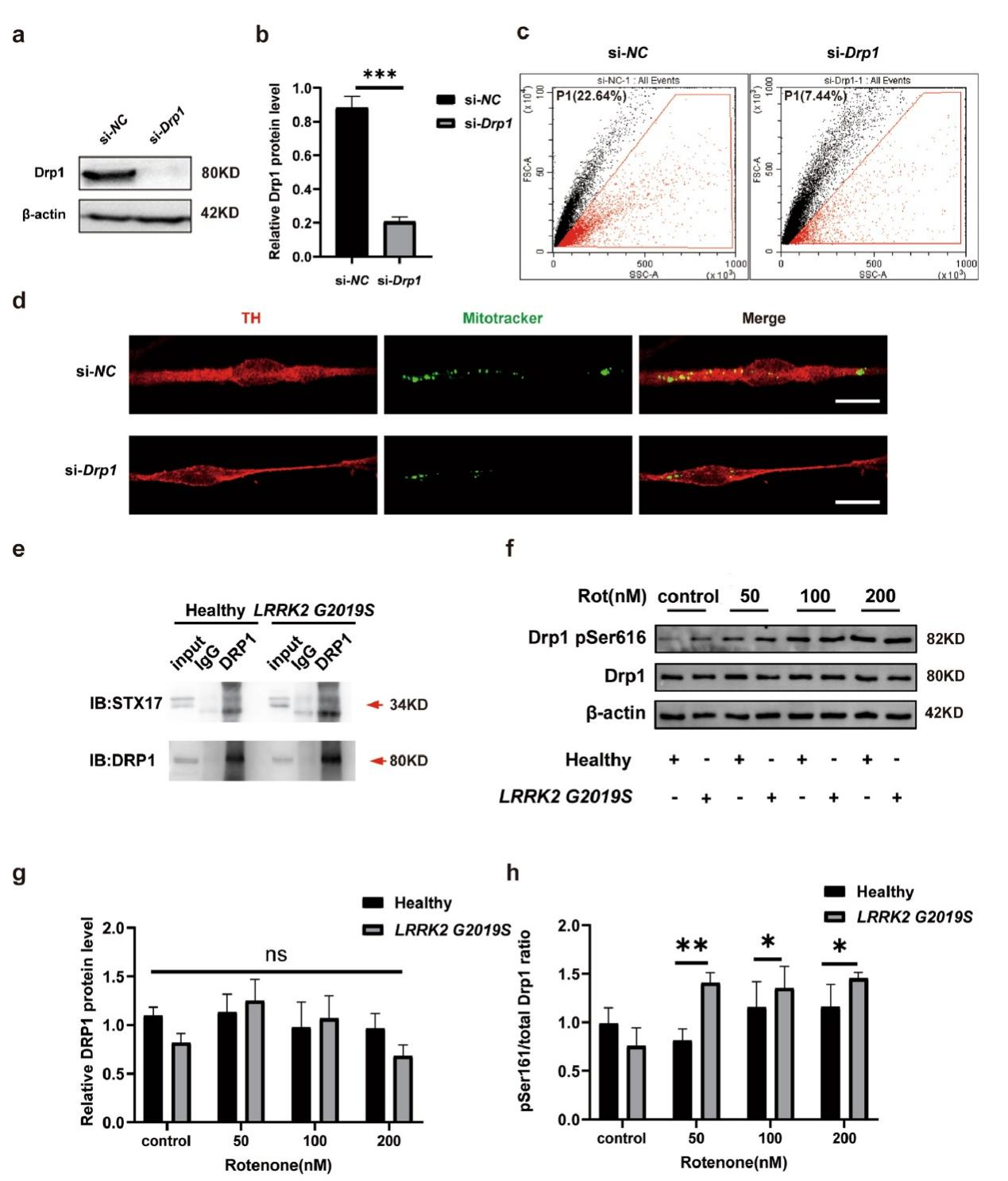
图4,Drp1参与STX17依赖的线粒体转移
5. LRRK2 G2019S突变与鱼藤酮处理联合影响Drp1 Ser616位点的磷酸化
在200 nM鱼藤酮处理的野生型和突变型星形胶质细胞中,LRRK2抑制剂PF-06447475仅显著降低突变型细胞的Drp1 pSer616水平,对野生型无显著影响。相比之下,Drp1磷酸化抑制剂DUSP6在两种基因型细胞中均能显著降低Drp1 pSer616水平,且呈剂量依赖性。总Drp1蛋白水平在各处理组间无显著变化。结果表明,DUSP6能有效抑制由LRRK2 G2019S突变和鱼藤酮共同诱导的Drp1过度磷酸化,适合用于后续的功能挽救实验。并比较了两种抑制剂对Drp1 Ser616磷酸化的影响,为后续挽救实验筛选出DUSP6。在200 nM鱼藤酮处理的星形胶质细胞中,LRRK2抑制剂PF-06447475仅显著降低突变型细胞的Drp1 pSer616水平,对野生型无显著影响。而Drp1磷酸化抑制剂DUSP6在两种基因型细胞中均能剂量依赖性地显著降低Drp1 pSer616水平,总Drp1蛋白水平无变化。结果表明,DUSP6能有效抑制由LRRK2 G2019S突变和鱼藤酮共同诱导的Drp1过度磷酸化,适合用于后续的功能挽救实验。
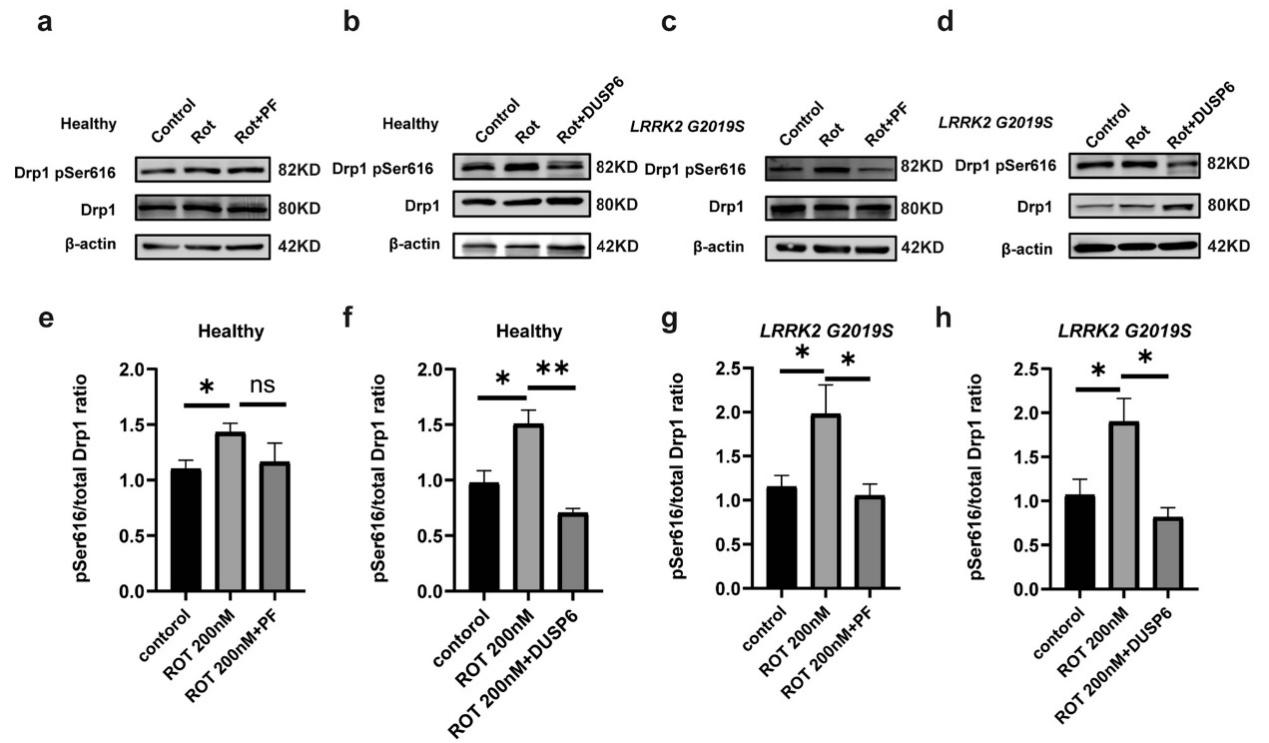
图5,Drp1抑制剂DUSP6可降低野生型和LRRK2 G2019S突变型星形胶质细胞中Drp1 pSer616的水平
6. DUSP6挽救受损的线粒体转移和多巴胺能神经元损伤
在200 nM鱼藤酮处理下,STX17与TOM20共定位减少(野生型降37.7%,突变型降46%),而DUSP6处理后共定位显著增加(野生型增37%,突变型增50%)。Western blot验证STX17蛋白水平变化,但明确其线粒体靶向能力受Drp1磷酸化调控。功能上,DUSP6使线粒体转移效率提高(野生型增27%,突变型增53%),神经元树突长度改善(野生型增12%,突变型增111%)。结果表明,DUSP6通过抑制Drp1 Ser616磷酸化,阻止STX17从线粒体脱落,恢复线粒体转移功能,对突变型神经元具有显著保护作用。
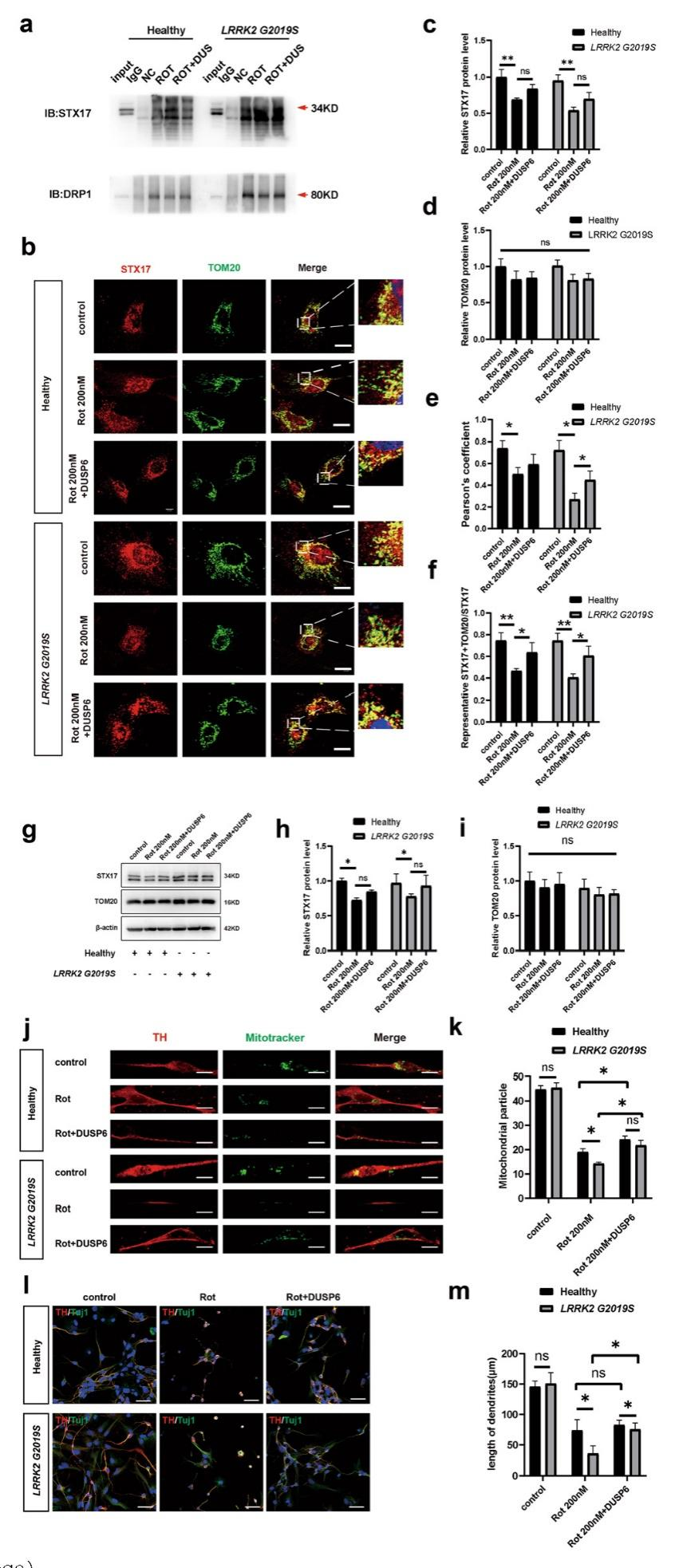
图6,DUSP6可挽救野生型和表达LRRK2 G2019S的星形胶质细胞中受损的线粒体转移和多巴胺能神经元损伤
7. 全文总结
研究揭示LRRK2 G2019S突变通过Drp1-STX17通路损害星形胶质细胞向多巴胺能神经元的线粒体转移功能,从而加剧环境毒素诱导的神经元损伤。研究发现,突变与鱼藤酮协同增强Drp1 Ser616磷酸化,导致STX17从线粒体外膜脱落,线粒体释放减少;而Drp1磷酸化抑制剂DUSP6可恢复STX17线粒体定位、提高线粒体转移效率并保护神经元。并将线粒体转移功能障碍确立为LRRK2突变致帕金森病的新机制,提出Drp1-STX17轴为治疗靶点,并证实DUSP6的神经保护作用。然而研究基于单例中国患者来源的iPSC,样本量有限,且LRRK2 G2019S在中国人群罕见,研究结果向其他人群或其他LRRK2突变类型的普适性有待验证。