 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站! 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站!各位读者好,今天为大家带来一篇使用整合乳酸化、多种组学分析以及分子生物学技术并结合动物、细胞和临床样本来验证p300介导的组蛋白乳酸化通过抑制线粒体自噬促进线粒体ROS积累,增强多巴胺受体激动剂(DAs)在泌乳素瘤中疗效的高分文章,是由华中科技大学研究团队2026年2月在Redox Biology发表的,题为“p300-mediated histone H3K18 lactylation promotes mitochondrial ROS accumulation via mitophagy inhibition to potentiate dopamine agonists efficacy in prolactinomas”。深入探究了p300介导的组蛋白乳酸化的机制,以及p300激活剂YF-2与多巴胺受体激动剂(DAs)联用可增强抗瘤效果,为DAs耐药泌乳素瘤提供新治疗策略。

发表杂志:
《Redox Biology》是氧化还原生物学领域的同行评审期刊,创刊于2013年,聚焦氧化还原信号调控、氧化应激与疾病机制等核心方向,是生命科学(尤其是生物化学、分子生物学、病理生理学及药物研发领域)科研人员的重要学术交流平台。

2025 年影响因子:11.9
ISSN:2213-2317
中科院分区:大类:生物(1 区 Top);小类:生物化学与分子生物学(1 区)、细胞生物学(1 区)
发文量:每年出版文章数平均约373篇
发表成本:APC为3,900美元(约2.8万人民币),作为中科院1区TOP期刊,性价比相对合理
审稿周期:该期刊以高效审稿著称,从投稿到接收平均仅需37 天,大多数作者反馈审稿周期在1-3 个月范围,远快于同类高影响因子期刊
《Redox Biology》作为氧化还原生物学领域的 Top 期刊,其高影响因子、严格的审稿标准、广泛的学科覆盖 使其成为该领域原创研究和综述的重要发表平台。对于从事以下研究的科研人员,尤其投稿:
1.氧化应激与疾病(癌症、神经退行性疾病、心血管疾病等)的机制研究;
2.抗氧化药物 / 制剂的细胞 / 动物实验验证;
3.redox 信号通路、线粒体 redox 代谢的分子机制探究;
4.氧化还原相关检测技术或组学分析方法的创新。
研究背景:
泌乳素瘤是常见的功能性垂体腺瘤,多巴胺受体激动剂(DAs)是一线治疗药物,但约10-30%患者会产生耐药,临床管理困难。既往研究多聚焦于多巴胺D2受体(DRD2)表达降低,而作者前期发现耐药患者肿瘤组织中p300表达减少,且p300通过调控DRD2转录影响DAs敏感性。近年研究表明p300介导的组蛋白乳酸化在基因转录、肿瘤增殖及耐药中起关键作用,且ROS水平与泌乳素瘤耐药相关。因此,本研究旨在探索p300通过组蛋白乳酸化调控线粒体ROS和线粒体自噬以增强DAs疗效的机制,为耐药泌乳素瘤提供新的治疗靶点。
该研究探讨了p300介导的组蛋白H3K18乳酸化通过抑制线粒体自噬促进线粒体ROS积累,从而增强多巴胺受体激动剂(DAs)在泌乳素瘤中的疗效。研究发现DAs通过抑制cAMP/PKA/CREB通路下调p300,而p300的上调或激活可通过H3K18la上调Ndufs7和Washc1,分别增加线粒体ROS生成和抑制线粒体自噬,终协同DAs诱导肿瘤细胞凋亡。p300激活剂YF-2与DAs联用可增强抗瘤效果,为DAs耐药泌乳素瘤提供新治疗策略。
研究框架:
1.提出问题:
基于临床观察到DAs耐药患者p300表达降低,且p300与DAs剂量负相关,提出“上调或激活p300能否增强DAs疗效”的核心问题。
2. 研究框架:
从临床样本分析p300与DAs响应的关系,到细胞和动物模型验证p300对DAs的增效作用,再通过分子机制探索p300-H3K18la-Ndufs7/Washc1轴调控线粒体ROS和自噬的通路。
3. 研究方法:
采用免疫组化、免疫荧光、Western blot、基因编辑、RNA测序、CUT&Tag、ChIP-qPCR、 Seahorse代谢分析、流式细胞术、Co-IP、GST pull-down及动物模型等多技术手段。
4. 分析数据:
通过相关性分析、差异表达基因筛选、通路富集、分子互作验证等解析p300调控线粒体ROS和自噬的机制。
5. 研究结论:
验证p300-H3K18la-Ndufs7/Washc1轴通过促进线粒体ROS积累和抑制自噬增强DAs疗效,确认p300激活剂YF-2的协同作用。

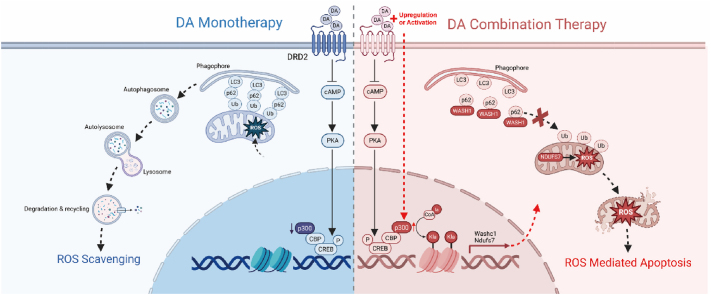
Fig.机制示意图
结果解析:
1. 多巴胺通过抑制cAMP/PKA/CREB通路下调p300表达
临床样本显示多巴胺(DA)耐药泌乳素瘤中p300表达降低,且与DA剂量负相关。动物模型和细胞实验证实DA通过抑制cAMP/PKA/CREB通路减少p300核定位,提示p300下调可能参与DA耐药机制。
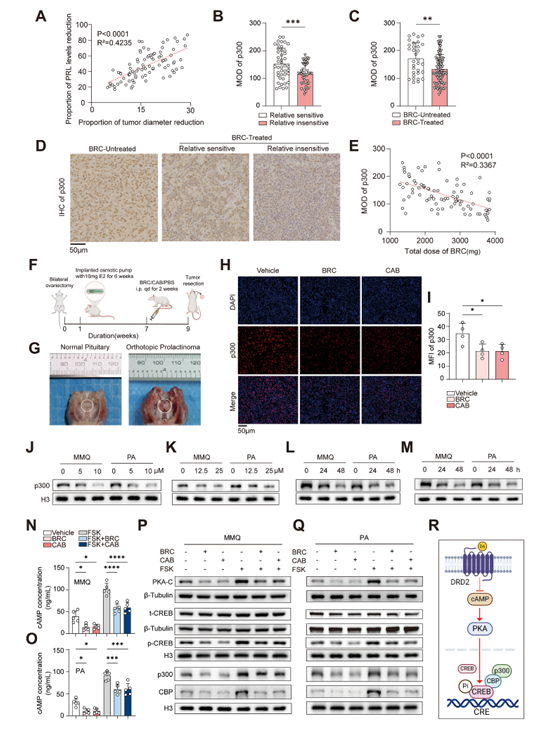
2. p300上调协同DA通过增加线粒体ROS促进肿瘤细胞凋亡
过表达或激活p300可增强DA的抗肿瘤效果,伴随线粒体ROS积累。ROS清除剂(NAC、GSH)可逆转凋亡,且p300的HAT结构域突变消除ROS升高和凋亡效应,表明p300通过HAT活性调控线粒体ROS介导DA敏感性。
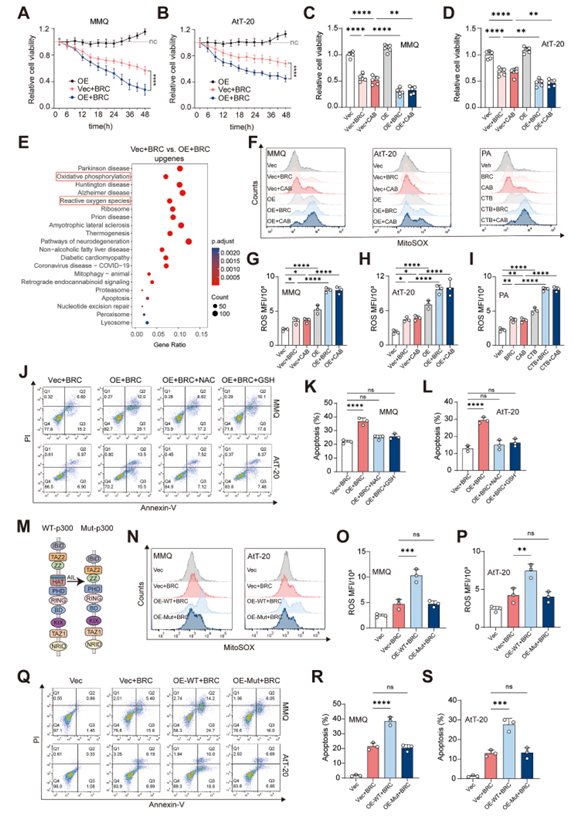
3. p300上调协同DA促进组蛋白H3K18乳酸化
p300上调联合DA诱导肿瘤细胞代谢向糖酵解转变,乳酸积累作为底物增强p300介导的组蛋白H3K18乳酸化(H3K18la)。HAT结构域突变或乳酸生成抑制可阻断H3K18la,提示H3K18la是p300调控ROS的关键表观遗传机制。
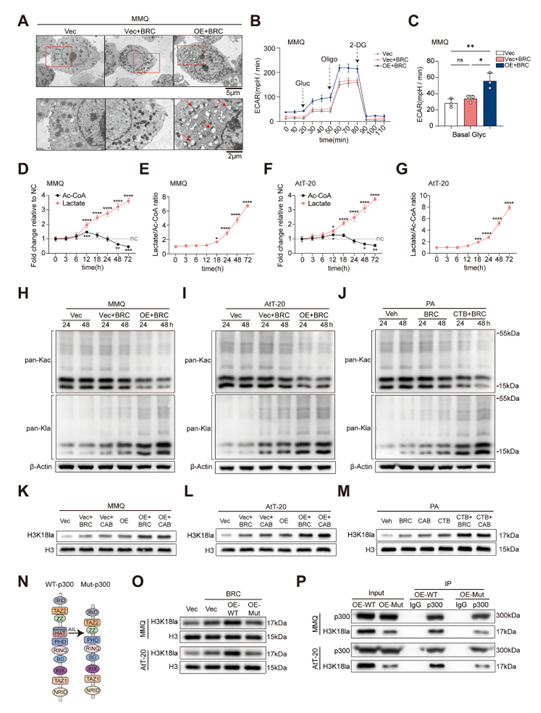
4. p300-H3K18la通过转录激活Ndufs7和Washc1升高线粒体ROS
CUT&Tag和RNA-seq显示H3K18la靶向激活Ndufs7和Washc1。Ndufs7上调增加线粒体复合体I电子泄漏,Washc1抑制线粒体自噬,二者共同导致ROS积累。双敲除Ndufs7和Washc1可显著逆转ROS和凋亡表型。
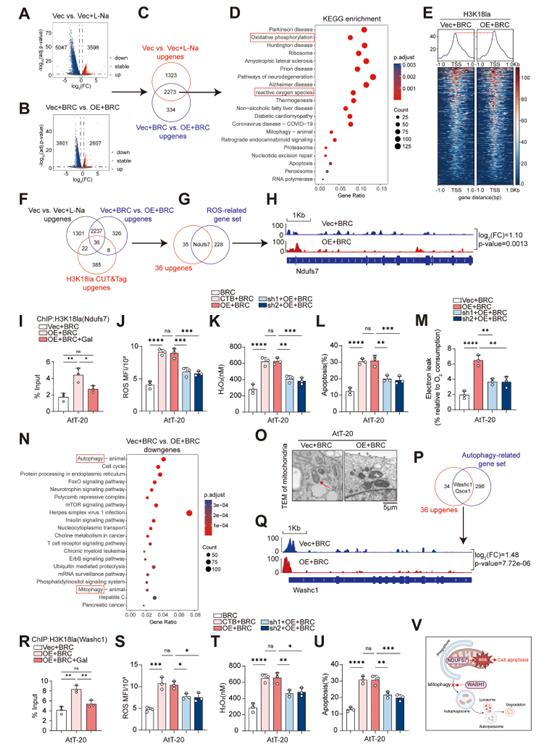
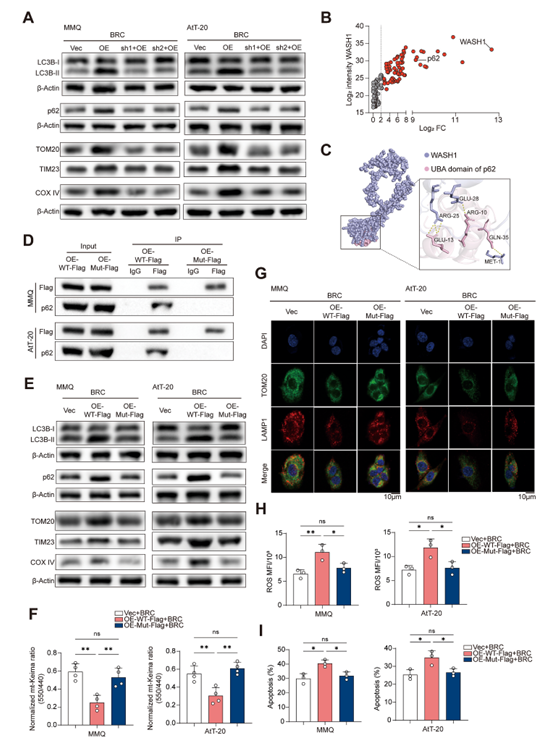
5. WASH1通过结合p62的UBA结构域抑制线粒体自噬
WASH1与p62的UBA结构域结合,阻断p62识别泛素化受损线粒体,抑制线粒体自噬。WASH1突变体(R25/E28位点)无法结合p62,恢复线粒体自噬和ROS清除,证实WASH1-p62相互作用是线粒体自噬抑制的关键
6. p300激活剂YF-2与DA协同抑制垂体腺瘤生长
YF-2(p300 HAT激活剂)与DA联合显著降低细胞活力、减少肿瘤体积,其效果依赖p300 HAT活性。机制上,YF-2增强H3K18la并上调Ndufs7/Washc1,促进线粒体ROS积累和凋亡,且无明显体内毒性。

研究结论:
p300通过H3K18la上调Ndufs7和Washc1,分别促进线粒体ROS生成和抑制线粒体自噬,从而增强DAs对泌乳素瘤的疗效。p300激活剂YF-2与DAs联用可协同抗肿瘤,为DAs耐药患者提供潜在治疗策略。
研究的创新性:
发现p300-H3K18la-Ndufs7/Washc1轴调控线粒体ROS和自噬的机制;揭示WASH1通过结合p62 UBA结构域抑制线粒体自噬的新功能;验证p300激活剂YF-2与DAs的协同抗瘤作用。
研究的不足之处:
未排除CBP等其他表观调控因子的潜在作用;YF-2的体内药代动力学和安全性未深入评估;Ndufs7上调导致ROS增加的具体分子机制(如复合体I功能变化)需进一步验证。
研究展望:
探索p300-H3K18la在其他垂体腺瘤中的作用;优化YF-2的结构以提高靶向性和降低脱靶效应;研究Ndufs7调控线粒体ROS的分子细节及WASH1-p62互作的结构基础;开展p300激活剂与DAs联用的临床试验。
研究意义:
阐明p300介导的组蛋白乳酸化在DAs增效中的作用机制,为解决泌乳素瘤DAs耐药问题提供新靶点和联合治疗策略,具有重要的临床转化价值。